中國(guó)經(jīng)(jīng)濟(jì)網(wǎng)(wǎng)北京6月21日訊(記者 郭文培) 6月20日�����,國(guó)家藥監(jiān)局發(fā)(fā)布通告�����,10批次藥品不符合規(guī)定���������。其中���,標(biāo)示四川逢春制藥有限公司生產(chǎn)(chǎn)的藥品又在列���。此前���,該公司生產(chǎn)(chǎn)的其他品種也曾出現(xiàn)過(guò)(guò)質(zhì)(zhì)量缺陷�������。
通告顯示���������,經(jīng)(jīng)湖南省藥品檢驗(yàn)檢測(cè)研究院檢驗(yàn)�������,標(biāo)示為四川逢春制藥有限公司生產(chǎn)(chǎn)的1批次玄麥甘桔顆粒(批次:210910)不符合規(guī)定�������,不符合規(guī)定項(xiàng)目為含量測(cè)定�����。
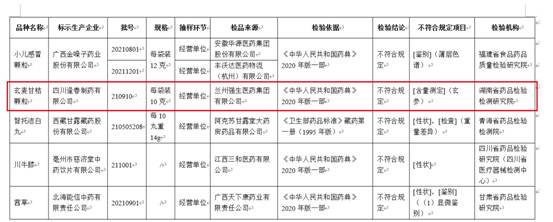
含量測(cè)定系指用規(guī)定的試驗(yàn)方法測(cè)定原料及制劑中有效成分的含量����,一般可采用化學(xué)(xué)���������、儀器或生物測(cè)定方法�。國(guó)家藥監(jiān)局表示������,對(duì)上述不符合規(guī)定藥品�����,藥品監(jiān)督管理部門(mén)(mén)已要求相關(guān)(guān)企業(yè)(yè)和單位采取暫停銷(xiāo)(xiāo)售使用�����、召回等風(fēng)(fēng)險(xiǎn)控制措施�,對(duì)不符合規(guī)定原因開(kāi)(kāi)展調(diào)查并切實(shí)(shí)進(jìn)(jìn)行整改������。
事實(shí)(shí)上�����,這并非四川逢春制藥有限公司首次出現(xiàn)藥品質(zhì)(zhì)量缺陷�������。中國(guó)經(jīng)(jīng)濟(jì)網(wǎng)(wǎng)記者查詢(xún)(xún)發(fā)(fā)現(xiàn)��������,此前該公司生產(chǎn)(chǎn)的益母草顆粒就曾被通報(bào)不合格�����。
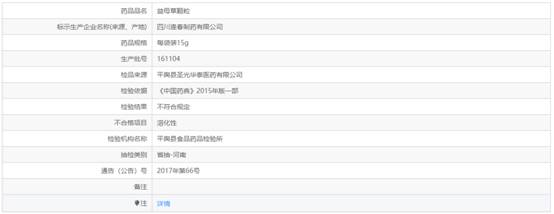
四川逢春制藥有限公司官網(wǎng)(wǎng)介紹�����,其始創(chuàng)(chuàng )于1973年�����,2000年由原中江制藥廠(chǎng)改制后完成戰(zhàn)略重組?����,F(xiàn)已形成集醫(yī)藥科研�����、工業(yè)(yè)生產(chǎn)(chǎn)�、醫(yī)藥商業(yè)(yè)���、農(nóng)業(yè)(yè)種養(yǎng)���、大健康產(chǎn)(chǎn)業(yè)(yè)��������、項(xiàng)目投資為一體的大型現(xiàn)代化民營(yíng)(yíng)集團(tuán)企業(yè)(yè)�����。幾十年來(lái)(lái)�����,憑借出色的品牌運(yùn)營(yíng)(yíng)和綜合實(shí)(shí)力����,其先后榮獲“四川省企業(yè)(yè)技術(shù)(shù)中心” “中國(guó)馳名商標(biāo)”�������、“全國(guó)醫(yī)藥行業(yè)(yè)十大放心用藥企業(yè)(yè)”��、 “全國(guó)醫(yī)藥行業(yè)(yè)百佳百姓放心品牌企業(yè)(yè)”��������、 “國(guó)家高新技術(shù)(shù)企業(yè)(yè)”等近百項(xiàng)榮譽(yù)(yù)����。
